V práci sú popísané možnosti využitia biotechnológií pri uchovávaní genetických živočíšnych zdrojov prostredníctvom kryokonzervácie pomocou vitrifikácie – veľmi rýchleho zmrazovania oocytov a embryí. Taktiež popisuje niektoré faktory zvyšovania kryotolerancie oocytov a embryí a ich odolnosti voči mrazeniu použitím nových kryoprotektív, antioxidantov a rastových faktorov.
Preživateľnosť oocytov po rozmrazení a preimplantačný vývoj embryí hovädzieho dobytka in vitro zlepšujú makromolekuly niektorých cytokínov ako sú – fibroblastový rastový faktor II (FGF-II), leukemický inhibičný faktor (LIF) a inzulínu podobný rastový faktor I (IGF-I). Využívanie preimplantačnej genetickej diagnostiky (PGD) chromozomálnych aberácií a sanitárnych postupov za účelom eliminácie patogénov pomôže zabezpečiť selekciu zdravých oocytov a embryí a zamedzí tak prenosu patogénov a geneticky podmienených ochorení na potomstvo.
Kryokonzervácia embryí zvierat ako biotechnická metóda, ktorá sa začala rozvíjať v 70. rokoch minulého storočia má dnes významné uplatnenie nielen vo výskumnej, ale aj praktickej sfére. Široké možnosti jej uplatnenia sú v oblasti zachovania genetickej biodiverzity, hlavne ohrozených druhov hospodárskych, ale aj divožijúcich zvierat formou dlhodobého uchovávania v génovej banke. Príkladom môžu byť snahy o záchranu nosorožca bieleho severného pomocou tvorby hybridných embryí in vitro (IVP), a to oplodnením oocytov príbuzného nosorožca bieleho južného, zmrazeným semenom nosorožca bieleho severného, na projekte ktorého sa úspešne podieľali aj pracovníci ZOO Dvůr Králové. V komerčnej sfére to môže mať uplatnenie pri uskladnení embryí zvierat vynikajúcej genetickej kvality a v ich medzinárodnom obchode. Obzvlášť významné sú technológie skladovania oocytov a embryí v súvislosti so starostlivosťou o ochranu a kontrolu zdravia zvierat.
Biotechnologické programy zamerané na uchovanie genetických zdrojov hospodárskych zvierat v súčasnosti využívajú kryokonzerváciu gamét, embryí a somatických buniek, tkanív semenníkov a vaječníkov uskladnených v génovej banke. Avšak na udržanie heterozygótnosti a integrity populácie je potrebné zmraziť nielen početnejšiu populáciu embryí ohrozených druhov, ale aj diferencovať odlišnosti zmrazovania kryosenzitívnych druhov embryí získaných napr. od ošípaných a koní. Tiež embryá produkované in vitro majú po rozmrazení, v porovnaní s in vivo embryami, výraznejšie zmeny organel buniek embryoblastu a trofoblastu, ktoré sú nezlučiteľné s ich životaschopnosťou.
Pri oocytoch musia metódy zmrazovania zabezpečiť vysokú životaschopnosť pre ich ďalšie využitie. Oocyty bezprostredne izolované z vaječníkov, alebo in vitro maturované oocyty v štádiu metafázy II, sú veľmi citlivé na zmrazovanie kvôli nízkemu pomeru povrchu k ich celkovému objemu, preto voda a kryoprotektívne látky nemôžu permanentne prechádzať cez cytoplazmatickú membránu. Okrem toho, zmrazovanie maturovaných oocytov môže viesť k narušeniu meiotického vretienka a chromozomálnym abnormalitám. Zmrazovanie maturovaných oocytov v štádiu metafázy II spôsobuje zlomy mikrotubúl vretienka a dezintegráciu chromozómov, čo prináša variabilné výsledky vzhľadom na problémy, ktoré vznikajú počas oplodnenia a embryonálneho vývoja. Životaschopnosť a vývojovú kompetenciou oocytov po zmrazení je preto potrebné overiť embryonálnym vývojom oocytov po ich oplodnení in vitro.
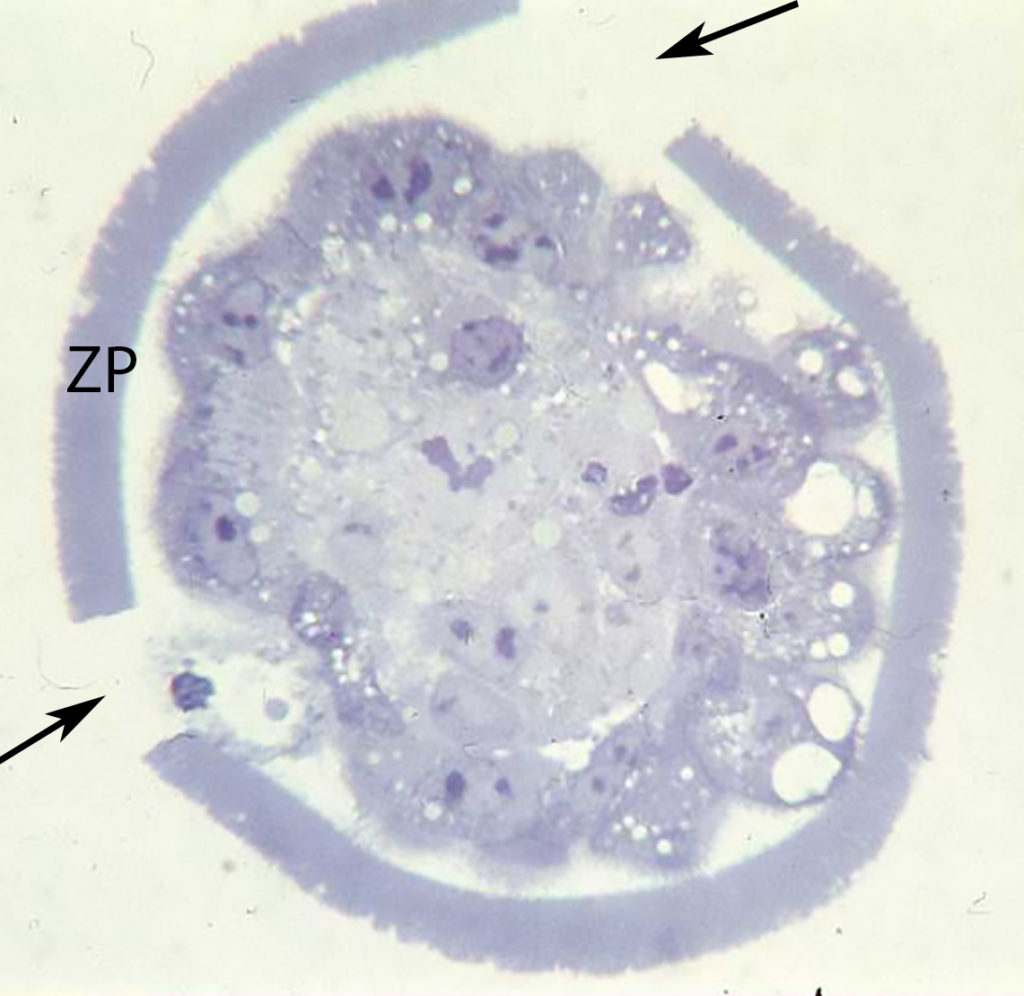
Pri štúdiu ultraštruktúry organel embryí po rozmrazení sme zistili, že nízke teploty spôsobujú v ich bunkách porušenie celistvosti membrán organel rôznej intenzity. Procesom zmrazovania dochádza k zvýšenému výskytu lyzozómov a multivezikulárnych teliesok a k porušeniu štruktúr aktínových filamentov cytoskeletu. Tieto zmeny spôsobujú poruchy biochemizmu a homeostázy embryí, čo v konečnom dôsledku vedie k zníženej plodnosti.
Aj napriek týmto neúspechom technológia kryouchovávania oocytov a embryí hospodárskych zvierat sa v poslednom čase dostáva do popredia. V tomto smere sa okrem klasickej metódy pomalého zmrazovania stále častejšie uplatňujú metódy vitrifikácie – rýchleho mrazenia, ktoré znižujú výskyt deštrukčných vnútrobunkových kryštálikov.
Banky samčích a samičích gamét a embryí zvierat významnou mierou prispievajú k ochrane genetickej diverzity ohrozených druhov a plemien. Za týmto účelom sa v súčasnosti pomerne úspešne využívajú biotechnologické postupy in vitro produkcie (IVP) embryí hovädzieho dobytka a ich kryokonzervácie. Napriek snahám zlepšiť postupy IVP embryí, pozorujeme v bunkách trofoblastu zvýšený výskyt vezikúl, na povrchu riedku populáciu mikroklkov, zníženú sieť medzibunkových spojení a zvýšený obsah lipidových kvapiek. Okrem toho, po ich zmrazení je prítomné trvalé poškodenie celistvosti membrán bunkových organel a zvýšený výskyt lyzozomálnych štruktúr. Tieto zmeny sa následne podieľajú na zníženej kvalite embryí a prispievajú k zníženiu ich kryotolerancie. Použitie rastových faktorov/cytokínov znižuje následky týchto poškodení, zvyšuje ich preživateľnosť a vývojovú schopnosť. Zlepšovanie odolnosti IVP embryí voči zmrazovaniu je stále aktuálna úloha, ktorej riešenie prispeje k zefektívneniu použitia ďalších biotechnologických metód zvyšujúcich využiteľnosť reprodukčného potenciálu zvierat. Aj keď bolo do súčasnej doby urobených mnoho štúdií za účelom objasnenia potenciálneho zdravotného rizika spojeného s embryotransferom a k nemu sa vzťahujúcim technológiám u zvierat, sú potrebné ďalšie výskumy orientované na riziko prenosu vírusových agensov a chromozómových aberácií oocytov a embryí, aby sa mohol zabezpečiť ich zdravotný status a nerušený vývoj.*
Prof. MVDr. Juraj Pivko, DrSc., RNDr. Alexander Makarevič, DrSc., Ing. Lucia Olexíková, Ph.D., Ing. Linda Dujíčková, RNDr. Elena Kubovičová, Ph.D., Národne poľnohospodárske a potravinárske centrum (NPPC), Výskumný ústav živočíšnej výroby Nitra, Slovenská republika