Nemožnost vyléčit vrozenou genetickou chorobu je minulostí. Veřejnost si ani neuvědomuje, že posledních několik let to v molekulární biologii doslova vře. Na svět se dostaly nové techniky, které umožňují editovat genom. Zjednodušeně řečeno – můžeme dnes již přepsat genetickou informaci jakéhokoli organismu v jakémkoli místě (genu) a to v zárodečných buňkách nebo i v buňkách určité tkáně dospělého organismu.
Požádali jsme v této souvislosti o rozhovor našeho předního biologa a popularizátora vědy prof. Ing. Jaroslava Petra, DrSc., z VÚŽV v Praze Uhříněvsi, který předsedá České komisi pro nakládání s GMO.
Vrátil jsem se z konference v USA, kde jsem se dozvěděl, že zažíváme tzv. CRISPRové šílenství. Je to skutečně tak pane profesore?
Ano, prožíváme revoluční období. Jsme na tom podobně, jako když Watson s Crickem v roce 1953 objevili dvojitou šroubovici DNA a pochopili jsme, jak to s tou dědičností vlastně funguje. Nebo když se podařilo vytvořit první rekombinantní DNA – sestavit genový konstrukt. Tehdy, v roce 1975, se uskutečnila v Asilomaru v Kalifornii konference, kdy se vědci dohadovali, jestli vůbec výzkum dál smí pokračovat.
Můžete tedy krátce představit techniky, které přicházejí dnes?
Nikdy jsem se nebál GMO, ale od května 2015 se jich bojím – brzy vysvětlím proč.
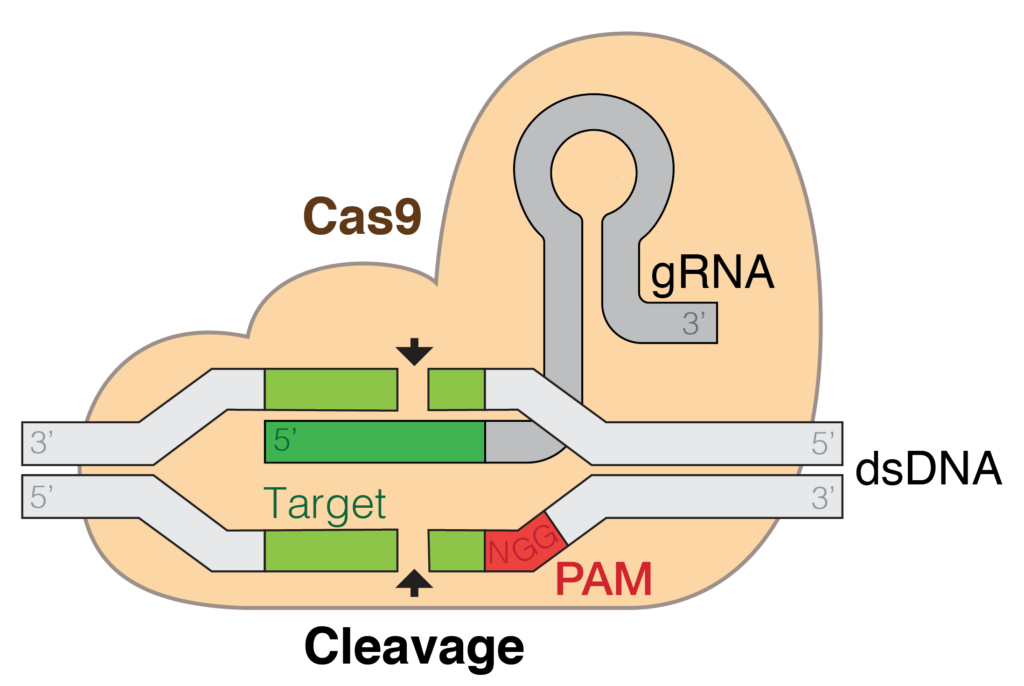
Zjednodušeně řečeno, nejvíce se používají tři techniky editace genomu – zinc-finger nukleázy, TALENy a CRISPRy. Nejnovější a nejrychleji se rozvíjející je technika, která nese celý název CRISPR–Cas 9. Je poměrně jednoduchá – zvládne ji hravě každý student molekulární biologie a je především levná a nabízí velmi široké použití.
Na jedné straně můžete udělat mutaci, která kopíruje přírodní mutaci. Můžete tam vnést jinou sekvenci, která do druhu nepatří, nebo která tam patří. Příkladem jsou bezrozí holštýni. S tím nemám problém, stejného výsledku bychom dosáhli klasickým šlechtěním, ale třeba za 150 let.
Další možností je vymazat nějaký gen nebo vnést gen cizí. Tady záleží na tom, o co konkrétně se jedná. Je třeba být opatrný a udělat řadu laboratorních zkoušek, které se týkají např. alergenity a předpokládat možné důsledky.
CRISPRem je ale možné zasáhnout do dědičné informace lidského embrya. Pokud je embryo předurčené k dědičné chorobě, jsme schopni to opravit. Tam nastupuje otázka nejen biologického, ale také etického přístupu.
Zmínil jste, že od roku 2015 máte obavy z genetických modifikací…
Ano – jde o případ tzv. gene drivů nebo také chcete-li mutagenních řetězových reakcí. Existují CRISPRy, které se šíří populací samy. Vnesený gen má schopnost vnášet sám sebe na nová přesně zvolená místa dědičné informace. V každé buňce těla se navodí stejná mutace také u druhého výtisku genu na homologním chromozómu. Při dědění gene drivu nevzniká obvyklý heterozygot, ale nositelé jsou opět homozygoti. To přepíše celou populaci do několika generací.
Stačí, aby unikla jedna jediná pozměněná ryba, jedna octomilka – jakmile najde sexuálního partnera, šíří se vnesený gen populací až do chvíle, kdy tam vznikne mutant, který nedovolí zabudování CRISPRu na cílové místo.
To by mohlo najít využití v boji proti škůdcům…
Samozřejmě, praktické využití by to našlo. U včel bychom mohli rozšířit populací geny varroatolerance nebo geny odolnosti vůči neonikotinoidům či dalším pesticidům. Vědci mají v laboratořích komáry, které když vypustíme do přírody, vznikne populace nepřenášející malárii. Máme i komáry, kteří nepřenáší virus zika. Nikdo si to ale nedovolí – neví se, jaké ekologické následky to může mít. Jak se říká: „Vystřelený šíp už nikdo nevrátí a spuštěný gene drive také ne.“
Jak tedy k novým technologiím typu CRISPR přistupovat?
Nechtěl bych, aby to vyznělo jednostranně. V některých případech je to banalita, v některých případech bychom měli před uvedením do praxe více prozkoumat souvislosti a v jiných případech bychom měli být nadmíru opatrní.
S CRISPR technologiemi dnes pracují studenti v diplomových pracích. Gene drive teoreticky může vzniknout nedopatřením – student si jen něco neuvědomí a vytvoří jej, aniž by o tom věděl.
Jsou tady ještě tzv. Do-it-yourself biologists. Je to sociální skupina lidí vzdělaná v biologii Pronajmou si byt jako laboratoř a koupí za pakatel vybavení od zkrachovalých biotechnologických firem. Takoví lidé často uvažují zvláštně a jsou prakticky nekontrolovatelní. Asi před pěti lety (technologie CRISPR ještě byla v plenkách), jsem měl telefonát: „Uděláme E. coli, která fluoreskuje, namnožíme ji a rozstříkáme na Karlově náměstí v parku. Pak to natočíme a uveřejníme na youtube – uvidíte ten cvrkot. Půjdete do toho s námi?“ …
Upozornil jsem je tedy, že jde o porušení zákona o GMO a hrozí jim až pětimilionová pokuta. Zřejmě jsem jim to rozmluvil, Karlák od té doby nesvítil.
Za těchto souvislostí nelze vyloučit, že někoho napadne, aby světlušky svítily růžově, a myšlenku promění v praxi. Pak takové transgenní světlušky vypustí.
Vraťme se ke smysluplnému využití. Lze tedy pomocí technologie CRISPR opravovat dědičnou chorobu jako např. diabetes i za života jedince?
Oprava dědičné choroby za života neboli genová terapie se již dělá běžně u řady nemocí. I CRISPR se pro to začíná používat. Princip spočívá v tom, že vezmete dospělci jeho buňky, namnožíte je a pustíte na buněčnou kulturu příslušný nástroj genového inženýrství. Úspěšná mutace se může povést u jedné buňky z milionu, ale lze ji najít a namnožit. Poté se buněčná kultura s upraveným genomem vpíchne pacientovi do těla – vydrží mu to po zbytek života.
Dnes existuje řada genových terapií, které léčí nádory. Např. vědci pozmění nádorovou buňku tak, že je citlivá na léčiva, která předtím nezabírala.
Pokud jde o diabetes I. typu, kdy imunitní systém zničí pacientovi jeho vlastní buňky produkující inzulín, lze v těle pozměnit jiné buňky slinivky tak, aby se naučily inzulín vyrábět a staly se jakýmisi „náhradníky“. Tyhle buněčné náhradníky imunitní systém neničí, protože je „vysazený“ pouze na tzv. beta-buňky Langerhansových ostrůvků, které mají produkci inzulínu na starosti ver zdravém organismu. Zatím se daří takhle léčit diabetes I. typu u laboratorních myší. Ale na první klinické zkoušky zřejmě nebudeme dlouho čekat. Než se však léčba stane standardním postupem, uteče ještě hodně času.
Jak moc už lze tyto metody využívat prakticky?
V EU je zatím povolena jedna jediná genová terapie Glybera – pro dědičnou poruchu metabolismu tuků. Je to však vzácná choroba, proto za pět let od jejího povolení byl vyléčen pouze jeden člověk.
V klinických zkouškách jsou ale desítky genových terapií – zhoubné nádory mozku, prostaty, slinivky a další. Jsou vyvinuty postupy, kdy se vezmou bílé krvinky pacienta a zmodifikují tak, aby napadaly rakovinné buňky. Poté se vrátí do těla pacientovi. Tak se daří léčit leukémie.
Jaká je současná situace v legislativě kolem nových technik vedoucích ke genetickým modifikacím?
Pokud jde o GMO, systém je univerzální pro celou EU. Legislativa musí být harmonizovaná. Řídíme se evropskou směrnicí, se kterou musí být kompatibilní náš zákon. Máme to svým způsobem jednodušší, než asistovaná reprodukce, tam by se Evropa nedohodla.
V současnosti o technice CRISPR rozhoduje Soudní dvůr Evropské unie jako instituce nejvyšší. Když dvůr vynese rozsudek, nejede přes to vlak. Vydává také předběžná stanoviska – to už je na světě. Hovoří o tom, že by se na mutace touto technikou neměla vztahovat evropská GMO legislativa. Zároveň ale není právní prostředek, který by zabránil členským zemím EU, aby si to samy zakázaly.
Pokud bude existovat rozhodnutí na evropské úrovni, že nejde o GMO, dovedu si představit, že se najdou země – Rakousko, Polsko, Francie, které prohlásí, že to je GMO. Vzájemnou obchodní výměnu takových komodit mezi členskými zeměmi si lze jen těžko představit.
Můžete mít herbicid-tolerantní plodinu, která je vytvořena podle seznamu A, a druhou stejně tolerantní vyrobenou podle seznamu B. Obě budou odolné vůči témuž herbicidu, ale každá bude podléhat jinému režimu. To je samo o sobě Kocourkov, ale nikoli ten největší.
Horší je, že vznikají stále nové techniky včetně výše zmíněných, které nejsou zařazené ani na jeden ze seznamů. To je problém. EU jmenovala před pár lety expertní výbor, který se pokusil nové techniky zařadit do seznamů. Po prvních sedmi ale vyhlásil tento výbor stop-stav. Dnes jsou tyto techniky již zastaralé, ustupují CRISPRům a TALENům, které v době práce expertní komise neexistovaly. V seznamu tedy nemáme ani jednu aktuální techniku.
Jak tedy můžete jako Česká komise pro nakládání s GMO pracovat? Máte nějaký návrh rozumného řešení?
Já si myslím, že by se měl zohlednit fenotyp – to znamená výsledná vlastnost geneticky modifikovaného organismu. Na tomto principu ale naše česká GMO komise jednotlivé případy již řeší. Na základě technik vznikají organismy s určitými vlastnostmi. Pokud organismus nenarušuje životní prostředí, nemá vliv na zdraví lidí zvířat a rostlin, není důvod, proč by se nemělo s organismem za nějakých podmínek nakládat.
Ve chvíli, kdy se do genomu vnáší něco cizího, je třeba obezřetnost. Např. u sexovaného kura společnosti eggXYt to bude zřejmě fluoreskující protein buď z medúzy nebo z korálovce. Jde tedy o bílkovinu, která tam normálně není. Pak by mne zajímalo, jestli není alergenní, nebo za některých okolností toxická a podobně. Nechal bych vše projít schvalovacím systémem.
Evropa dosud nevnímala zkostnatělý systém kolem GM organismů jako problém. Ani gene drive Evropa nepovažovala na prvořadý problém – eurokomisař doslova řekl, že se to nebude přednostně řešit.
Ve chvíli, kdy svět na to najede a nebude tuto techniku považovat za GMO, tak EU vytvoří bariéru. Tu si ale nemůžeme dovolit – jsme závislí na krmivech.
Naše legislativa není jednoduchá – klade důraz ne techniky a nemůže zareagovat na jejich rychlý vývoj. Evropa se dostává do právního vakua. Pokud soudní dvůr rozhodne, že CRISPR není GMO, pak se ale může stát, že někdo bude tuto technologii využívat a komisi pro nakládání s GMO to nebude ani hlásit, zákon tím neporuší. GMO komise o nich nebude vědět a nikdo pak neposoudí možné riziko.*
(Kompletní rozhovor s Jaroslavem Petrem najdete v Našem chovu 8/2018)